Decisão da ANVISA inclui nova faixa etária no uso do Mounjaro para tratamento de diabetes tipo 2
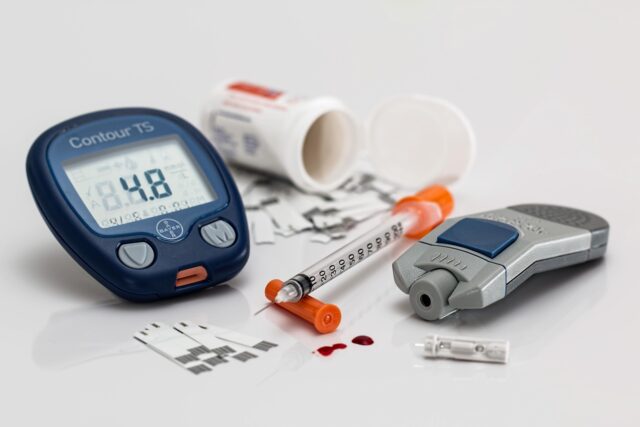
A rotina de quem convive com diabetes tipo 2 costuma envolver atenção diária, consultas e decisões sobre tratamento. Por isso, qualquer mudança nas opções disponíveis chama atenção. Foi o que aconteceu com o medicamento Mounjaro, que agora teve o uso ampliado no Brasil.
Vale ressaltar que a decisão veio da Agência Nacional de Vigilância Sanitária (Anvisa) e permite que o Mounjaro também seja utilizado por crianças e adolescentes a partir de 10 anos.
Até então, o uso era voltado apenas para adultos. Essa atualização abre um novo caminho para famílias que lidam com o diagnóstico mais cedo.
O que muda com a liberação do Mounjaro
Com a nova autorização, por meio da Resolução-RE nº 1.592, o Mounjaro passa a ser uma opção também para pacientes mais jovens com diabetes tipo 2.
Isso significa que médicos podem considerar o uso do medicamento dentro de um plano de cuidado para essa faixa etária.
No entanto, é importante sinalizar que a ampliação não acontece de forma automática. Antes de pontuar essa decisão, a Agência Nacional de Vigilância Sanitária analisa estudos que mostram como o remédio funciona, além de avaliar pontos ligados à segurança e ao efeito esperado.
Esses dados vêm de estudos que mostram como o medicamento age no organismo, quais resultados foram observados e quais cuidados precisam ser considerados. Só depois dessa etapa é que a ampliação pode ser autorizada.
No caso do Mounjaro, essa avaliação permitiu incluir pacientes a partir de 10 anos. Mesmo assim, o uso segue a orientação médica, que considera o histórico de cada pessoa.
Dessa forma, o Mounjaro continua com as indicações anteriores, mas agora inclui esse novo grupo.
Segundo dados da Sociedade Brasileira de Diabetes, no país existem aproximadamente 213 mil adolescentes vivendo com diabetes tipo 2, e quase 1,5 milhão com pré-diabetes.
Outras discussões sobre medicamentos da mesma classe
Além da liberação do Mounjaro para um novo público, a Anvisa também discute regras sobre medicamentos da mesma linha.
Inclusive, uma proposta em análise trata da forma como esses produtos podem ser manipulados. A ideia é definir critérios para etapas como armazenamento, transporte e controle de qualidade.
O foco é garantir a segurança de pacientes que utilizam medicamentos injetáveis de GLP-1 (Peptídeo Semelhante ao Glucagon-1), conhecidos como canetas emagrecedoras, com princípios ativos de semaglutida, tirzepatida e liraglutida.
Esses medicamentos são conhecidos por muitas pessoas por conta do uso ligado ao controle de peso, mas também têm papel no tratamento de doenças como o diabetes tipo 2.
Em suma, o debate sobre essas regras busca organizar melhor o uso e garantir que os produtos sigam padrões definidos. Isso inclui desde a origem dos insumos até a forma como chegam ao paciente.
Com informações da Agência Nacional de Vigilância Sanitária (Anvisa)